周期表とは
皆さんも学生時代には必死に暗記しませんでしたか?
「スイヘーリーベーボクノフネ・・・」とかw苦労しましたよね^^;
すべての物質は、とっても小さい粒子が集まってできてて、物質を構成する基本的な粒子が原子。
原子は正の電荷を持つ原子核と、負の電荷を持つ電子からできている。
元素とは何でしょうか?昔、勉強した化学式を思い出してみてください。
水=? + ?
さて、上の化学式の?部分は一体何でしたっけ?覚えてますか?
私たちが生きるに欠かせない”水”、それを電気分解すると水素と酸素に分けられます。
上の化学式の解答はこちら・・・H₂O=H₂ + O
ここまで書いたら皆さん、もうお分かりですね!そうです原子とは物質を構成する
粒子のことをいいますが、元素とはその原子の種類のことをいいます。
端的に書いちゃうと、H₂O = H₂ +Oってことです!!
水は水素原子と酸素原子からできた分子で、元素としては「水素」と「酸素」という
名称を指すわけです。

”原子”とひと言でいっても現在、発見されているだけで118種類あります。
その、ひとつひとつを元素といいます。なので、周期表とはこの”原子の種類”を
表した表になります。原子は陽子・中性子・電子という組み合わせから成り立っていて
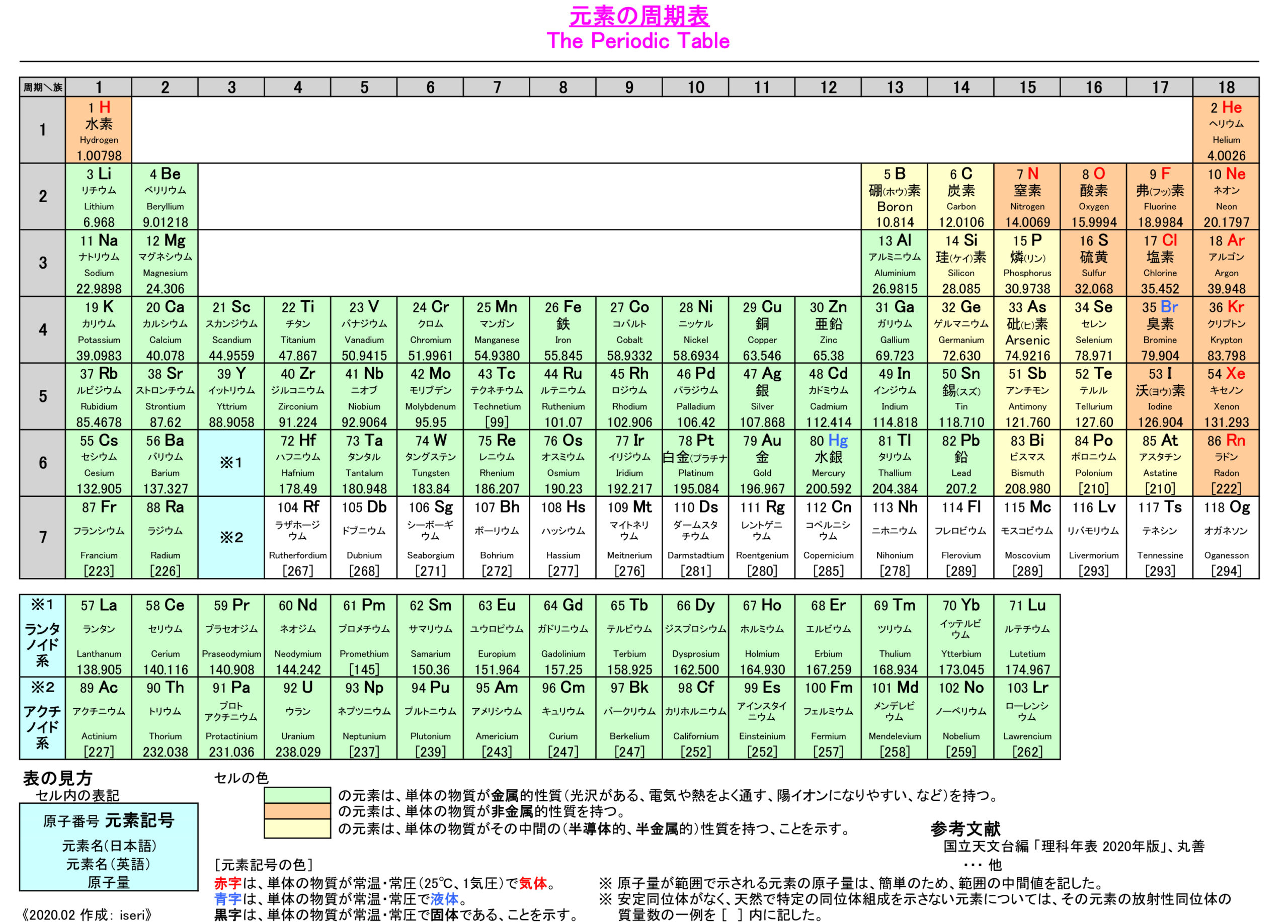
各元素はこの陽子や中性子、電子の数が異なります。下の周期表の最初にある水素は
原子番号(陽子の数=電子の数)1番で、1.00798と書かれているのは原子量です。
周期表によっては、原子量ではなく質量数(陽子の数+中性子の数)で
書かれている表もあります。
※質量数と原子量などの違いは質量欠損や同位体など複雑な話になるのでココでは避けます※
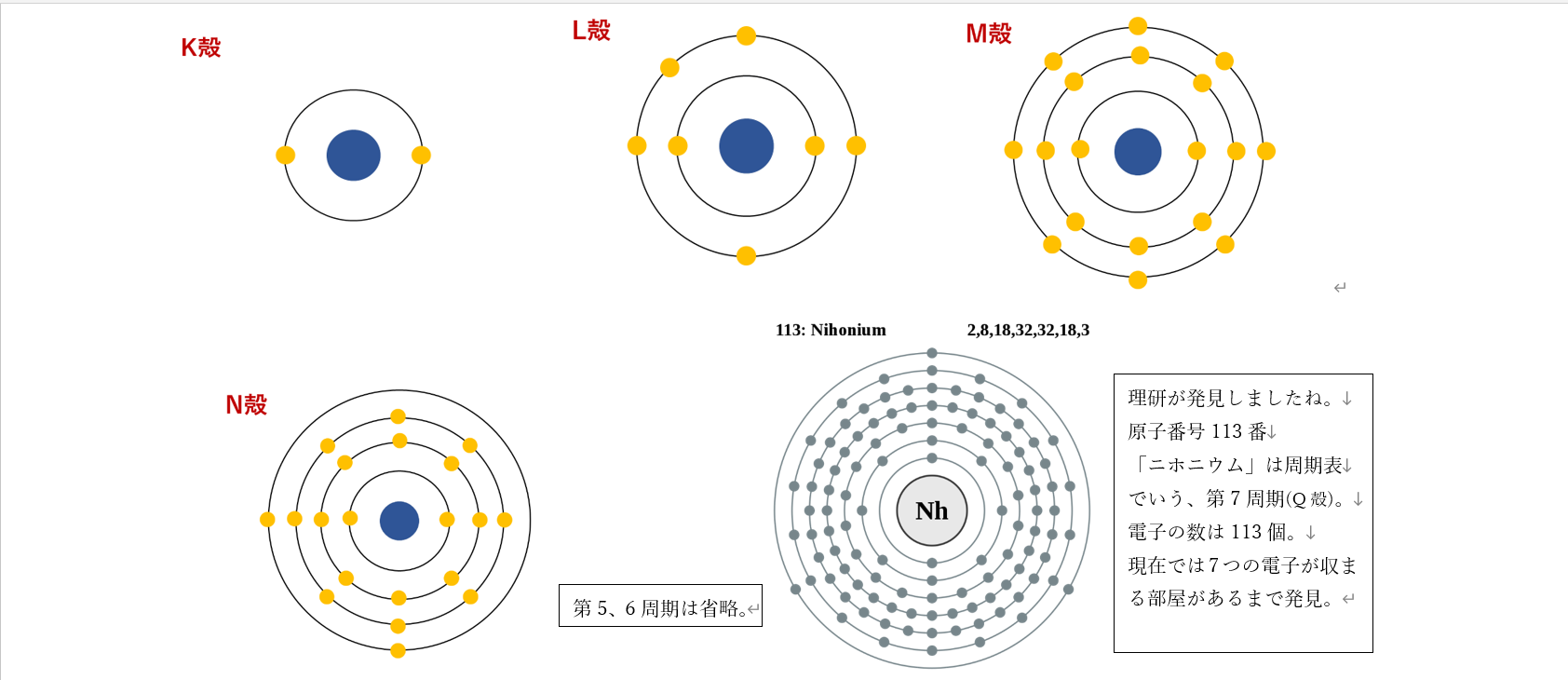
★周期(表を横に見る)は1~7周期まであります。これは原子の周りを回っている
「電子」の”居場所”を示してます。
電子というのは無暗やたらに飛び回っている訳じゃないんです!実はお行儀が良くて、決まった所を
決まった定員で回っています。
原子核に近い部屋から、第1周期(K殻)、次は第2周期(L殻)・・・と呼ばれ順番に電子は入ってるよ。
つまり、最後の第7周期とは原子核から7周目まで部屋(殻)があるということです!
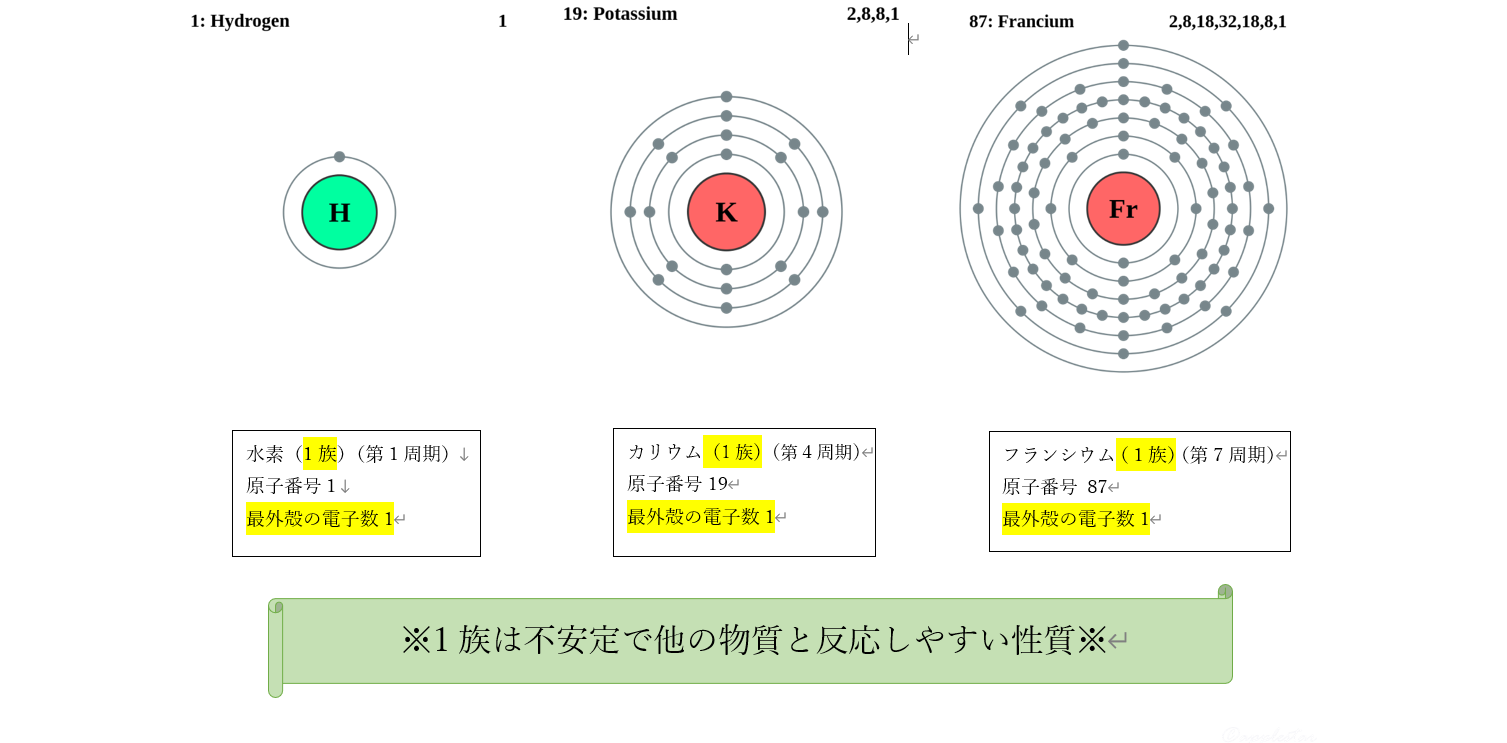
★族(表を縦に見る)は、1~18族まであります。これが何を表すかというと、似たような
”性質”の元素の集まり!ってことです。その性質を決めるポイントは、一番外側の部屋(殻)にある
電子の数が同じ(ヘリウムを除く)ということ。
性質ごとに分類されている
最近の周期表は更に見易くなっていて、特徴を見分けできる工夫がされています。
先述した様に縦で見る”族”で性質が異なります。基本的なものをご紹介しましょう。
☆アルカリ金属→ほかの物質と非常に反応しやすいです。電池などに多く使用されてます。(1~2族)
★アルカリ土類金属(BeとMg除く)→カルシウムは人類にとって体内に潜む最も多い金属元素。(2族)
☆典型元素→原子番号が増えると最外殻の電子数も増える。
★遷移元素→縦(族)だけではなく、隣の元素とも似た様な性質を持つ元素。
☆超ウラン元素→U(ウラン)より原子番号が大きい。93番以降の元素。ウランは天然元素だが、
以降は基本的に人工的に作られた元素です。
★ランタノイド→57~71番の元素で希土類(レアアース)元素とも呼ばれています。
☆アクチノイド→89~103番の元素。いずれも放射性元素で物理的、化学的によく似た性質をもつ。
★超アクチノイド→104~現在発見されてる最後の元素118番のオガネゾンまでの超重元素。
現在未発見の119番以降の元素もこれにあたります。
(※但し、周期は8~と増えていきます)
おわりに
今回はapplestarの大好きな周期表について少しだけ触れてみました。
まだまだ未発見の元素があり、暫定名ですがお決まりの、ウン〇〇〇ウムが多いですが
これはIUPAC(国際化学連合)が決めている命名規則という数の読みがあるわけです!
下記の様になりますが、面白い名前ですよね。
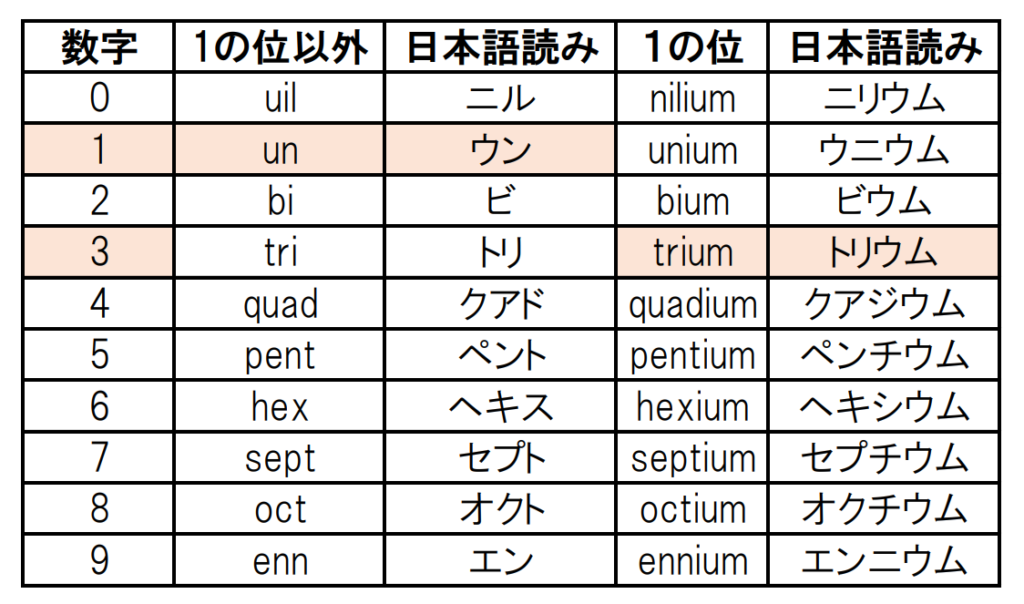
以前、理研が原子番号113番「ニホニウム」を発見し話題になりましたね。
名称が決まるまでの間は命名規則に基づき「ウンウントリウム」だったの知ってる?
なので119番以降の未発見元素の名称は、この表に基づいていますから
興味のある方は照らし合わせてみると面白いですよ^^
このブログを読んで少しでも周期表に興味をもって頂けたら幸いです。
ではでは、applestarでしたぁ💛バイバーイ(@^^)/~~~✨



コメントをどうぞ